Alessio Nencioni, Irene Caffa, Salvatore Cortellino
Resumo | A vulnerabilidade das células cancerosas á privación de nutrientes e á súa dependencia de metabolitos específicos son as marcas emerxentes do cancro. As dietas de xaxún ou de fastidio (FMD) levan a amplas alteracións nos factores de crecemento e nos niveis de metabolitos, xerando ambientes que poden reducir a capacidade das células cancerosas para adaptarse e sobrevivir e así mellorar os efectos das terapias contra o cancro. Ademais, o xaxún ou a febre aftosa aumentan a resistencia á quimioterapia en células normais pero non cancerosas e promoven a rexeneración nos tecidos normais, o que podería axudar a previr os efectos secundarios dos tratamentos. Mentres os pacientes non toleran o xaxún, ambos os estudos clínicos e animais mostran que os ciclos de febre aftosa de baixa calor son viables e son seguros. Están en curso varios ensaios clínicos que avalían o efecto do xaxún ou febre aftosa en eventos adversos en tratamento e en resultados de eficacia. Propoñemos que a combinación de febre aftosa con quimioterapia, inmunoterapia ou outros tratamentos representa unha estratexia potencialmente prometedora para aumentar a eficacia do tratamento, evitar a adquisición da resistencia e reducir os efectos secundarios.
Os factores relacionados coa dieta e o estilo de vida son determinantes fundamentais do risco de desenvolver cancro, sendo certos cancros máis dependentes dos hábitos alimentarios que outros1�
Aínda que na última década fomos testemuñas de cambios sen precedentes e de avances notables no tratamento do cancro, 14,15, segue habendo unha necesidade crucial para ser máis eficaz e, posiblemente,
O xaxún obriga ás células saudables a entrar nunha división lenta e un modo altamente protexido que os protexe de insultos tóxicos derivados de medicamentos contra o cancro mentres sensibiliza os distintos tipos de células cancerosas a estes terapéuticos. Este descubrimento implica que unha única intervención dietética podería axudar a abordar aspectos diferentes e igualmente importantes da terapia do cancro.
Neste artigo de opinión, discutimos o argumento biolóxico para empregar dietas (xaxúns) de fasting ou de fasting (FMD) para emitir TEAEs pero tamén para previr e tratar o cancro. Tamén ilustran as advertencias deste enfoque experimental18,19 e os estudos clínicos publicados e en curso nos que se aplicaron xaxún ou FMD a pacientes con cancro.
Contidos
Resposta de xaxún sistémico e celular
O ayuno conduce a cambios na actividade de moitas rutas metabólicas asociadas ao cambio nun modo capaz de xerar enerxía e metabolitos usando fontes de carbono liberadas principalmente do tecido adiposo e en parte do músculo. Os cambios nos niveis de hormonas e metabolitos circulantes tradúcense nunha redución da división celular e actividade metabólica de células normais e, en última instancia, protexe-las de insultos quimioterapéuticos11,12. As células cancerosas, desobedeciendo as ordes anti-crecemento ditadas por estas condicións de fame, poden ter a resposta oposta ás células normais e, polo tanto, sensibilizarse á quimioterapia e outras terapias do cancro.
Resposta sistémica ao xaxún
A resposta ao xaxún é orquestada en parte polos niveis circulantes de glicosa, insulina, glucagón, hormona do crecemento (GH), IGF1, glucocorticoides
O glucagón e os baixos niveis de insulina tamén estimulan a degradación dos triglicéridos (que se almacenan principalmente no tecido adiposo) en glicerol e ácidos graxos libres. Durante o xaxún, a maioría dos tecidos utilizan ácidos graxos para obter enerxía, mentres que o cerebro depende da glicosa e dos corpos cetónicos producidos polos hepatocitos (os corpos cetónicos pódense producir a partir de acetil-CoA xerado a partir da ?-oxidación de ácidos graxos ou de aminoácidos cetoxénicos). Na fase cetoxénica do xaxún, os corpos cetónicos alcanzan concentracións no rango milimolar, normalmente comezando despois de 2 días desde o inicio do xaxún. Xunto co glicerol e os aminoácidos derivados da graxa, os corpos cetónicos alimentan a gliconeoxénese, que mantén os niveis de glicosa nunha concentración de aproximadamente 3 mM (4 mg por dl), que é maioritariamente utilizada polo cerebro.
Os glucocorticoides e a adrenalina tamén contribúen a dirixir as adaptacións metabólicas
Finalmente, o xaxún diminúe os niveis de leptina circulante, unha hormona feita predominantemente por adipocitos que inhibe a fame, ao tempo que aumenta os niveis de adiponectina, que aumenta a descomposición dos ácidos graxos. Así, en conclusión, as características da resposta sistémica dos mamíferos ao xaxún son os baixos niveis de glicosa e insulina, niveis elevados de corpos de glucagón e cetona, baixos niveis de IGF23,24 e leptina e altos niveis de adiponectina.
Resposta celular ao xaxún
A resposta das células sans ao xaxún consérvase evolutivamente e confire protección celular e, polo menos en organismos modelo, demostrouse que aumenta a vida útil e a saúde12,22,25. O IGF31
O xaxún e a restrición de glicosa resultante inhiben a actividade da PKA, aumentan a actividade da AMPK e activan a EGR1 e, polo tanto, conseguen efectos protectores das células, incluídos os do miocardio22,25,26. Por último, o xaxún e a fiebre aftosa (ver máis abaixo para a súa composición) tamén teñen a capacidade de promover efectos rexenerativos (cadro 1) por mecanismos moleculares, algúns dos cales estiveron implicados no cancro, como o aumento da autofaxia ou a indución da actividade da sirtuína22,37. .

Aproximacións dietéticas en febre aftosa
Os enfoques dietéticos baseados no xaxún que foron investigados máis extensamente en oncoloxía, tanto preclínica como clínicamente, inclúen o xaxún acuático (abstinencia de todos os alimentos e bebidas excepto a auga) e a fiebre aftosa11,12,17,25,26,50 (táboa). 60). Os datos clínicos preliminares indican que pode ser necesario un xaxún de polo menos 1 horas para lograr efectos clinicamente significativos en oncoloxía, como previr o dano do ADN inducido pola quimioterapia nos tecidos sans e axudar a manter
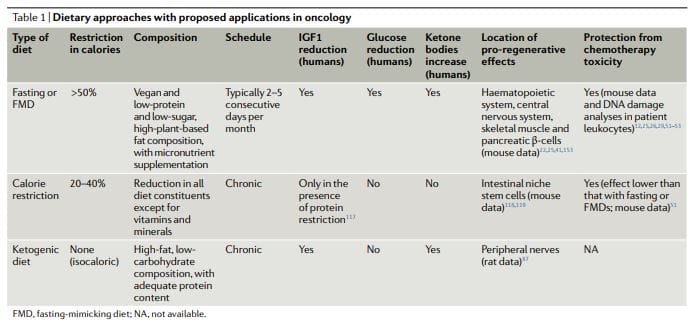
Non obstante, a maioría dos pacientes néganse ou teñen dificultades para completar o xaxún de auga, e os riscos potenciais da deficiencia prolongada de calorías e micronutrientes asociados a el son difíciles de xustificar. A fiebre aftosa son réximes dietéticos deseñados médicamente moi baixos en calorías (é dicir, normalmente entre 300 e 1,100 kcal por día), azucres e proteínas que recrean moitos dos efectos do xaxún só con auga pero cun mellor cumprimento do paciente e un risco nutricional reducido22,61,62, 3. Durante unha fiebre aftosa, os pacientes normalmente reciben cantidades ilimitadas de auga, pequenas porcións estandarizadas de caldos de vexetais, sopas, zumes, barras de froitos secos e tés de herbas, así como suplementos de micronutrientes. Nun estudo clínico de 5 ciclos mensuais dunha fiebre aftosa de 1 días en suxeitos xeralmente sans, a dieta foi ben tolerada e reduciu a graxa corporal total e no tronco, a presión arterial e os niveis de IGF62. En ensaios clínicos oncolóxicos anteriores e en curso, o xaxún ou a fiebre aftosa adoitan ser administrados cada 3 semanas, por exemplo, en combinación con réximes de quimioterapia, e a súa duración oscilou entre 4 e 1 días5. . É importante destacar que nestes estudos non se informaron eventos adversos graves (nivel G52,53,58,61,63 ou superior, segundo os Common Terminology Criteria for Adverse Events)68.
Dietas cetogênicas
As dietas cetogénicas (KD) son réximes dietéticos que teñen un contido normal en calorías, ricas en graxas e baixo en carbohidratos69,70. Nun KD clásico, a relación entre o peso da graxa e o peso combinado de hidratos de carbono e proteínas é de 4: 1. Cabe destacar que as febres aftomas son tamén cetogênicas porque teñen un alto contido en graxa e teñen a capacidade de inducir elevacións substanciais (? 0.5 mmol por litro) nos niveis de corpos cetónicos circulantes. Nos humanos, unha enfermidade cardíaca tamén pode reducir os niveis de IGF1 e insulina (máis dun 20% respecto aos valores iniciais), aínda que estes efectos están afectados polos niveis e tipos de hidratos de carbono e proteínas na dieta71. Os KD poden reducir os niveis de glicosa no sangue, pero normalmente permanecen dentro do rango normal (é dicir,> 4.4 mmol por litro) 71.
En particular, os KD poden ser eficaces para previr o aumento da glicosa e da insulina que se produce normalmente en resposta aos inhibidores de PI3K, o que se propuxo para limitar a súa eficacia72. Tradicionalmente, os KD utilizáronse para tratar a epilepsia refractaria, principalmente en nenos69. Nos modelos de rato, os KD inducen efectos anticanceríxenos, especialmente no glioblastoma70,72-86. Os estudos clínicos indican que os KD probablemente non teñan actividade terapéutica substancial cando se usan como axentes únicos en pacientes con cancro e suxiren que se deberían buscar beneficios potenciais destas dietas en combinación con outros enfoques, como quimioterapia, radioterapia, tratamentos antianxioxénicos, inhibidores de PI3K.
Informouse que as EK teñen efectos neuroprotectores nos nervios periféricos e no hipocampo87,88. Non obstante, aínda está por determinar se as enfermidades dixestivas tamén teñen efectos prerexenerativos similares ao xaxún ou ás febres aftose (recadro 1) e se as enfermidades dixitais tamén se poden usar para protexer aos mamíferos vivos da toxicidade da quimioterapia. En particular, os efectos rexenerativos do xaxún ou as febres aftose parecen maximizarse ao cambiar do modo de resposta á fame, que implica a degradación dos compoñentes celulares e a morte de moitas células e o período de realimentación no que sofren as células e os tecidos. reconstrución22. Debido a que as KD non forzan a entrada nun modo de inanición, non promoven unha degradación importante dos compoñentes e tecidos intracelulares e non inclúen un período de reabastecemento, é improbable que causen o tipo de rexeneración coordinada observada durante a reabastecemento da febre aftosa.
Restrición de calorías
Aínda que a restrición calórica crónica (RC) e as dietas deficientes en aminoácidos específicos son moi diferentes do xaxún periódico, comparten co xaxún e a fiebre aftosa unha restrición máis ou menos selectiva de nutrientes, e teñen efectos anticanceríxenos81,89�112. A RC normalmente implica unha redución crónica do 20% na inxestión de enerxía a partir da inxestión calórica estándar que permitiría a un individuo manter un peso normal30. É moi eficaz para reducir os factores de risco cardiovascular e a incidencia do cancro en organismos modelo, incluídos os primates113,114.
Non obstante, a CR pode causar efectos secundarios, como cambios no aspecto físico, aumento da sensibilidade ao frío, forza reducida, irregularidades menstruais, infertilidade, perda de libido, osteoporose, cicatrización máis lenta de feridas, obsesión alimentaria, irritabilidade e depresión. En pacientes con cancro, existe unha preocupación substancial de que poida agravar a desnutrición e que inevitablemente cause perda excesiva de masa corporal magra18,113�116. CR reduce os niveis de glicosa no sangue en xaxún, aínda que permanecen dentro do intervalo normal114. Nos humanos, a CR crónica non afecta os niveis de IGF1 a non ser que tamén se implemente unha restrición moderada de proteínas117.
Os estudos demostran que, reducindo a sinalización de mTORC1 nas células de Paneth, a CR aumenta a súa función de células nai e que tamén protexe as células nai intestinais de reserva de ADN. 118,119, pero non se sabe si os efectos pro-regenerativos noutros órganos tamén son provocados por CR. Así, os datos dispoñibles suxiren que o xaxún e as febras aftadas crean un perfil metabólico, rexenerativo e de protección que é distinto e probablemente máis potente que o provocado por un KD ou CR.
O xaxún e a febre aftosa en terapia: efectos sobre os niveis de hormonas e metabolitos
Moitos dos cambios nos niveis de hormonas circulantes e metabolitos que se observan normalmente en resposta ao xaxún teñen a capacidade de exercer efectos antitumorales (isto é, niveis reducidos de glicosa, IGF1, insulina e leptina e aumento dos niveis de adiponectina). ou para protexer os tecidos saudables contra os efectos secundarios (isto é, niveis reducidos de IGF23,120,121 e glicosa). Debido a que os corpos cetónicos poden inhibir as desacetilases de histonas (HDAC), o aumento dos corpos cetónicos inducido polo xaxún pode axudar a diminuír o crecemento do tumor e promover a diferenciación a través dos mecanismos epigenéticos.
Non obstante, demostrouse que o acetoacetato de corpos cetónicos acelera, en lugar de reducir, o crecemento de certos tumores, como os melanomas con BRAF123 mutado. Aqueles cambios para os que existe a evidencia máis sólida dun papel nos efectos beneficiosos do xaxún e da fiebre aftosa contra o cancro son as reducións dos niveis de IGF1 e glicosa. A nivel molecular, o xaxún ou a fiebre aftosa reducen as fervenzas de sinalización intracelular, incluíndo a sinalización IGF1R�AKT�mTOR�S6K e cAMP�PKA, aumenta a autofaxia, axuda ás células normais a resistir o estrés e promove a inmunidade contra o cancro25,29,56,124.
Resistencia ao estrés diferencial: aumento da tolerancia á quimioterapia
Algúns ortólogos de oncogeno de levadura, como Ras e Sch9 (ortólogo funcional de mamífero S6K), son capaces de diminuír a resistencia ao estrés nos organismos modelo 27,28. Ademais, na maioría dos cánceres humanos están presentes as mutacións que activan IGF1R, RAS, PI3KCA ou AKT ou que inactivan PTEN. Xuntos, isto levou á hipótese de que a fame causaría efectos opostos no cancro fronte ás células normais en canto á súa capacidade de soportar estresores celulares, incluíndo quimioterapia. Noutras palabras, a fame pode conducir
Segundo a hipótese DSR, as células normais responden á inanición regulando á baixa a proliferación asociada e a xenoxénese e / ou ensamblaxe de ribosomas, o que obriga ás células a entrar nun modo de autoservemento e as protexe dos danos causados pola quimioterapia, a radioterapia e outros axentes tóxicos. Pola contra, nas células canceríxenas, este modo de autocontentamento evítase a través de cambios oncoxénicos, que provocan a inhibición constitutiva das vías de resposta ao estrés12 (Fig. 1). Coherente co modelo DSR, a fame a curto prazo ou a eliminación do proto-oncoxene
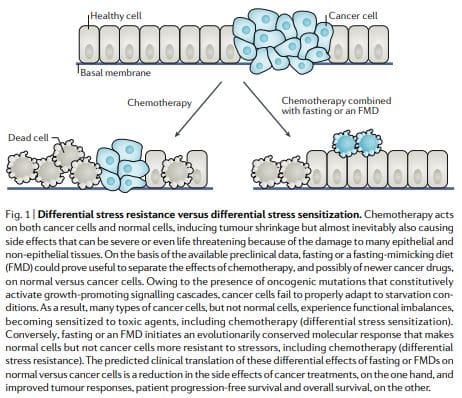
Resultados similares foron obtidos en células de mamíferos: a exposición a células de glia de rato primarias protexidas por medios de baixo contido de glicosa contra a toxicidade de peróxido de hidróxeno ou ciclofosfamida (unha quimioterapia prooxidante) pero non protexía as liñas celulares de cancro de rato, rata e glioma humano e neuroblastoma. Consistente con estas observacións,
Estudos posteriores descubriron que a redución da sinalización de IGF1 en resposta ao xaxún protexe a glía primaria e as neuronas, pero non as células de glioma e neuroblastoma, da ciclofosfamida e dos compostos pro-oxidantes e protexe os fibroblastos embrionarios de rato da doxorrubicina29. Os ratos con deficiencia de IGF1 hepático (LID), animais transxénicos cunha deleción condicional do xene Igf1 hepático que presentan unha redución do 70% nos niveis circulantes de IGF80 (niveis similares aos alcanzados por un xaxún de 1 horas en ratos)72, foron protexidos contra tres de cada catro fármacos de quimioterapia probados, incluída a doxorrubicina.
Os estudos de histoloxía mostraron signos de miopatía cardíaca inducida por doxorubicina só en ratos control tratados con doxorubicina pero non en ratos LID. En experimentos con animais portadores de melanoma tratados con doxorubicina, non se observou ningunha diferenza en termos de progresión da enfermidade entre os ratos control e LID, o que indica que as células cancerosas non estaban protexidas da quimioterapia por niveis reducidos de IGF1. Con todo, de novo, os ratos LID con tumores presentaron unha notable vantaxe de supervivencia en comparación cos animais de control debido á súa capacidade para soportar a toxicidade por doxorrubicina29. Así, en xeral, estes resultados confirmaron que a regulación descendente de IGF1 é un mecanismo clave polo que o xaxún aumenta a tolerabilidade á quimioterapia.
Os inhibidores de dexametasona e mTOR son amplamente utilizados no tratamento do cancro, xa sexa pola súa eficacia como antiemética e
Estas intervencións reducen a actividade da PKA ao tempo que aumentan a actividade da AMPK e, polo tanto, activan a EGR1, o que indica que a sinalización de cAMP� PKA media o DSR inducido polo xaxún a través de EGR1 (ref. 26). EGR1 tamén promove a expresión de péptidos cardioprotectores, como o péptido natriurético auricular (ANP) e o péptido natriurético de tipo B (BNP) no tecido cardíaco, o que contribúe á resistencia á doxorrubicina. Ademais, o xaxún e/ou a fiebre aftosa poden protexer os ratos da miocardiopatía inducida pola doxorrubicina aumentando a autofaxia, o que pode promover a saúde celular ao reducir a produción de especies reactivas do osíxeno (ROS) mediante a eliminación de mitocondrias disfuncionais e a eliminación de agregados tóxicos.
Ademais de reducir a toxicidade inducida pola quimioterapia nas células e aumentar a supervivencia dos ratos tratados con quimioterapia, os ciclos de xaxún inducen a rexeneración da medula ósea e evitan a inmunosupresión causada pola ciclofosfamida de forma relacionada coa PKA e relacionada co IGF1. Así, resultados convincentes preclínicos indican o potencial do xaxún e as febres aftose para aumentar a tolerabilidade á quimioterapia e evitar efectos secundarios importantes. Debido a que os datos clínicos iniciais prestan máis apoio a este potencial, estes estudos preclínicos constrúen unha forte razón para avaliar a febre aftosa en ensaios clínicos aleatorios con TEAE como punto final principal.
Sensibilización por estrés diferencial: aumentando a morte das células do cancro
Se se usa só, a maioría das intervencións na dieta, incluíndo xaxún e febre aftosa, teñen efectos limitados contra a progresión do cancro. De acordo coa hipótese de sensibilización por estrés diferencial (DSS), a combinación de xaxún ou febre aftosa cun segundo tratamento é moito máis prometedor. Esta hipótese prevé que, aínda que as células cancerosas son capaces de adaptarse a concentracións limitadas de osíxeno e nutrientes, moitos tipos de células cancerosas non son capaces de executar cambios que permitan a supervivencia no ambiente tóxico e deficiente de nutrientes xerado pola combinación de xaxoterapia e xexún. , por exemplo. Experimentos tempranos en cancro de mama, melanoma
Consideramos unha resposta inadecuada das células cancerosas ás condicións alteradas, incluída a redución dos niveis de IGF1 e glicosa causados polo xaxún ou por febre aftosa como mecanismo fundamental que subxace ao

Ao reducir a dispoñibilidade de glicosa e aumentar a oxidación de ácidos graxos, o xaxún ou as febres aftos tamén poden promover o cambio da glicólise aeróbica (efecto Warburg) á fosforilación oxidativa mitocondrial nas células cancerosas, que é necesaria para manter o crecemento das células cancerosas no ambiente máis pobre en nutrientes50 (Fig. 2). Este cambio leva a unha maior produción de ROS11 como resultado dunha maior actividade respiratoria mitocondrial e tamén pode implicar unha redución do potencial redox celular debido á diminución da síntese de glutatión a partir da glicólise e a vía de pentosa fosfato50. O efecto combinado do aumento do ROS e a redución da protección antioxidante aumenta o estrés oxidativo nas células cancerosas e amplifica a actividade dos quimioterapéuticos. En particular, debido a que unha alta actividade glicolítica demostrada pola alta produción de lactato é predictiva de agresividade e propensión metastásica en varios tipos de cancro129, os efectos anti-Warburg do xaxún ou a febre aftosa teñen o potencial de ser particularmente eficaces contra os cancros agresivos e metastáticos.
Ademais dun cambio no metabolismo, o xaxún ou as febras aftimas provocan outros cambios que poden promover o DSS nas células do cancro de páncreas. O xaxún aumenta os niveis de expresión de
Finalmente, o xaxún pode regular o receptor da leptina eo seu fluxo abaixo
En particular, é probable que moitos tipos de células canceríxenas, incluíndo AML29, poidan adquirir resistencia evitando os cambios metabólicos impostos polo xaxún ou a fiebre aftosa, unha posibilidade que se ve incrementada aínda máis pola heteroxeneidade metabólica que caracteriza a moitos cancros129. Así, un dos principais obxectivos para o futuro próximo será identificar os tipos de cancro que son máis susceptibles a estes réximes dietéticos mediante biomarcadores. Por outra banda, cando se combinan con terapias estándar, o xaxún ou a fiebre aftosa raramente provocaron a adquisición de resistencia en modelos de ratos cancro, e a resistencia ao xaxún combinada con quimioterapia tamén é pouco común en estudos in vitro, o que subliña a importancia de identificar terapias que, cando se combina con FMD, produce efectos tóxicos potentes contra as células cancerosas cunha toxicidade mínima para as células e tecidos normais11,17,50,55-57,59,124.
Potenciación da inmunidade antitumoral por xaxún ou febre aftosa
Datos recentes suxiren que o xaxún ou febre aftosa por si mesmos, e en maior medida cando se combina coa quimioterapia, desencadean a expansión dos proxenitores linfoides e promoven
Dietas contra o cáncer en modelos de rato
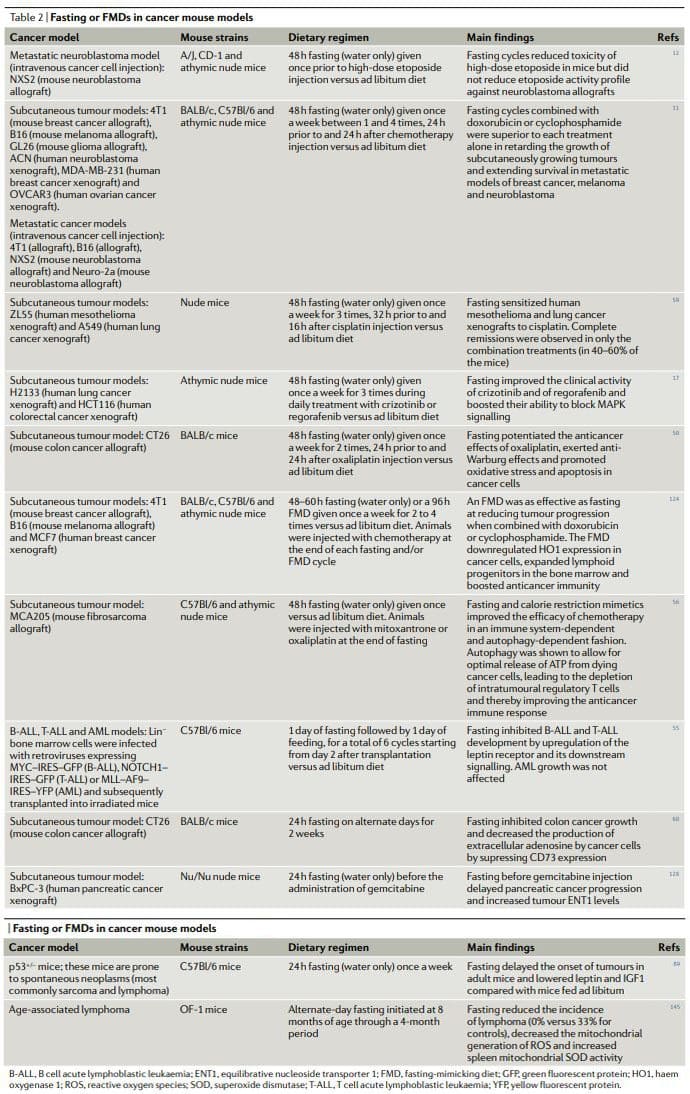
En xeral, os resultados de estudos preclínicos sobre o xaxún ou a febre aftosa en modelos de cancro animal, incluídos modelos para o cancro metastásico (táboa 2), demostran que o xaxún periódico ou as febres aftosa acadan efectos pleitrópicos contra o cancro e potencian a actividade de quimioterapéuticos e ITK mentres exercen efectos protectores e rexenerativos en múltiples órganos22,25. Para conseguir os mesmos efectos sen o xaxún e / ou a febre aftosa esixiríase primeiro a identificación e despois o uso de múltiples medicamentos eficaces, caros e frecuentemente tóxicos e probablemente sería sen a vantaxe de inducir unha protección celular sa. Chama a atención que en polo menos dous estudos o xaxún combinado coa quimioterapia demostrou ser a única intervención capaz de lograr regresións tumorais completas ou supervivencia a longo prazo nunha fracción consistente dos animais tratados11,59
As KD crónicas tamén mostran a
CR reduciu a tumorigénesis en modelos xenéticos de cancro de rato, modelos de rato con tumorigénesis espontánea e modelos de rato de cancro inducido por carcinóxenos, así como en monos91,92,97,98,101,102,104. Pola contra, un estudo descubriu que a CR a partir da mediana idade realmente aumenta a incidencia de neoplasias de células plasmáticas en ratos C106,108,109,136Bl/138. Non obstante, no mesmo estudo, a CR tamén estendeu a vida útil máxima aproximadamente un 57%, e o aumento observado na incidencia do cancro atribuíuse ao aumento da lonxevidade dos ratos sometidos a CR, a idade na que
É importante destacar que a CR mellorou a actividade do tratamento contra o cancro en varios modelos de cancro, incluída a actividade dun anticorpo antiIGF1R (ganitumab) contra o cancro de próstata141, ciclofosfamida contra células de neuroblastoma135 e inhibición da autofagia en xenotransplantes de células epiteliais renal HRAS-G12. Non obstante, CR ou KD en combinación con terapias contra o cancro parecen ser menos eficaces que o xaxún. Un estudo sobre o rato atopou que, a diferenza do xexún só, o CR só non foi capaz de reducir o crecemento dos gliomas de rato que cresen subcutáneamente GL100 e que, en contraste co xaxún a curto prazo, a CR non aumentou a actividade de cisplatino contra o peito subcutáneo de 26T4. tumours1. No mesmo estudo, o xaxún demostrou ser substancialmente máis eficaz que o CR e un KD ao aumentar a tolerabilidade doxorubicin51. Aínda que o xaxún ou unha febre aftosa, CR e KD probablemente actúan e modulen a superposición
A fase de realimentación podería entón
Xaxún e FMD en prevención do cancro
Os estudos epidemiolóxicos e os estudos en animais, incluíndo monkeys108,109,144, e os humanos dan soporte á idea de que a CR crónica e o xaxún periódico e / ou unha febre aftosa poderían ter efectos preventivos contra o cancro nos humanos. Non obstante, a CR pode dificilmente implementarse na poboación en xeral debido a problemas de conformidade e posibles efectos secundarios115. Deste xeito, mentres que as recomendacións baseadas en evidencias de alimentos que prefiren (ou evitar), así como recomendacións de estilo de vida para reducir o risco de cancro están a establecerseNNUMX, o obxectivo agora é identificar e, posiblemente, estandarizar réximes dietéticos ben tolerados con baixos ou non efectos secundarios e avalía a súa eficacia preventiva contra o cancro nos estudos clínicos.
Como se comenteu anteriormente, os ciclos de febre aftosa provocan unha baixa regulación de IGF1 e glicosa e regulación ascendente de IGFBP1 e corpos cetónicos, que son cambios similares aos causados polo xaxún e son biomarcadores da resposta en xaxún. Cando os ratos C22Bl / 57 (que se desenvolven espontaneamente)
Un estudo previo do xaxún de días alternos, que se realizou en ratos de mediana idade para un total de meses 4, tamén atopou que o xaxún reduciu a incidencia do linfoma, levándoo a partir do 33% (para os ratos de control) a 0% (en xaxún. animais) 145, aínda que por mor da curta duración do estudo non se sabe se este réxime de xaxún impediu ou simplemente atrasou o
Polo tanto, os resultados prometedores dos estudos preclínicos combinados cos datos clínicos sobre o efecto dunha febre aftosa nos factores de risco
Aplicabilidade clínica en oncoloxía
Publicáronse catro estudos de viabilidade de xaxún e febre aftosa en pacientes sometidos a quimioterapia. Nunha serie de casos de pacientes con 52,53,58,61 diagnosticados con varios tipos de cancro, incluíndo cancro de mama, próstata, ovario, útero, pulmón e esófago, que xaxún voluntariamente ata 10hours antes e / ou ata 140hours despois da quimioterapia, non se produciron efectos secundarios importantes xaxún doutra cousa que a fame e asombrosidade foron reportados56. Os pacientes (seis) sometidos a quimioterapia con e sen xaxún reportaron unha redución significativa de fatiga, debilidade e eventos adversos gastrointestinais durante o xaxún. Ademais, nos pacientes nos que se puido avaliar a progresión do cancro, o xaxún non impediu a redución inducida pola quimioterapia no volume tumoral ou nos marcadores tumorales. Noutro estudo, as mulleres 58 con HER13 (tamén coñecido como ERBB2) negativas, o cancro de mama etapa II / III recibindo taxotere neoadxuvante, adriamicina e ciclofosfamida (TAC) foron asignados aleatoriamente a 2h rápido (só auga) antes e despois do inicio da quimioterapia ou a nutrición segundo as pautas estándar.
O xaxún a curto prazo foi ben tolerado e reduciu a caída na conta media de eritrocitos e trombocitos aos 7 días da quimioterapia. Curiosamente, neste estudo, os niveis de? -H2AX (un marcador de dano ao ADN) aumentaron 30 minutos despois da quimioterapia en leucocitos de pacientes sen xaxún pero non en pacientes que xaxuaron. Nunha escalada de dose do xaxún en pacientes sometidos a quimioterapia baseada en platino, 20 pacientes (que foron tratados principalmente por cancro urotelial, ovárico ou de mama) foron aleatorizados para xaxún durante 24, 48 ou 72 horas (dividido como 48 horas antes da quimioterapia e 24 horas despois da quimioterapia ) 53. Cumpríronse os criterios de viabilidade (definidos como tres ou máis de cada seis suxeitos en cada cohorte que consumen? 200kcal por día durante o período rápido sen exceso de toxicidade). Toxicidades relacionadas co xaxún
Hai moi pouco tempo, realizouse un ensaio clínico cruzado aleatorio para avaliar os efectos dunha febre aftosa sobre a calidade de vida e os efectos secundarios da quimioterapia nun total de pacientes con cancro de mama ou ovario 34. A febre aftosa estaba composta por
Retos na clínica
O estudo do xaxún ou de febre aftosa en oncoloxía non está exento de preocupacións, especialmente en relación coa posibilidade de que este tipo de réxime dietético puidese precipitar a desnutrición, a sarcopenia,
Conclusións
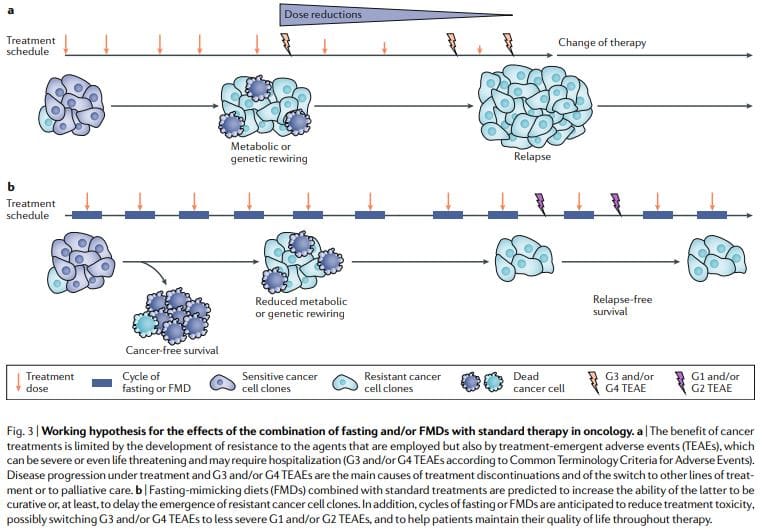
O xaxún periódico ou a febre aftosa amosan de forma consistente efectos anticancerosos en modelos de cancro de rato, incluída a capacidade de potenciar a quimiorradioterapia e os ITK e desencadear a inmunidade contra o cancro. Os ciclos de febre aftosa son máis factibles que os réximes dietéticos crónicos porque permiten aos pacientes consumir alimentos regularmente durante a febre aftosa, manter unha dieta normal entre ciclos e non producen unha perda de peso grave e posiblemente efectos prexudiciais sobre o sistema inmunitario e endócrino. En particular, como terapias autónomas, o xaxún periódico ou os ciclos de febre aftosa probablemente mostrarían unha eficacia limitada contra os tumores establecidos. De feito, en ratos, o xaxún ou a febre aftosa afectan a progresión dun número de cancros de xeito similar á quimioterapia, pero só, raramente coinciden co efecto obtido en combinación con medicamentos contra o cancro que poden producir unha supervivencia libre de cancro11,59. Así, propoñemos que é a combinación de ciclos periódicos de febre aftosa con tratamentos estándar a que ten o maior potencial para promover a supervivencia sen cancro en pacientes, como suxeriron os modelos de rato11,59 (Fig. 3).
Esta combinación pode ser particularmente potente por varias razóns: primeiro, os medicamentos contra o cancro e outras terapias poden ser eficaces, pero unha parte dos pacientes non responde porque as células cancerosas adoptan estratexias metabólicas alternativas que levan á supervivencia. Estes modos metabólicos alternativos son moito máis difíciles de soportar en condicións de xaxún ou febre aftosa debido ás deficiencias ou cambios na glicosa, certos aminoácidos, hormonas e factores de crecemento, así como noutras vías descoñecidas que levan á morte celular. En segundo lugar, o xaxún ou febre aftosa pode impedir ou reducir a adquisición de resistencia. En terceiro lugar, o xaxún ou febre aftosa protexen as células e os órganos normais dos efectos secundarios causados por unha gran variedade de medicamentos contra o cancro. Con base en evidencias preclínicas e clínicas de viabilidade, seguridade e eficacia (na redución de IGF1, graxa visceral
Ademais, é esencial aplicar a febre aftosa cunha comprensión dos mecanismos de acción desde a súa potencia
Os estudos clínicos en curso sobre a fiebre aftosa en pacientes con cancro63,65 proporcionarán respostas máis sólidas sobre se a prescrición de fiebre aftosa periódica en combinación con axentes anticanceríxenos convencionais axuda a mellorar a tolerabilidade e a actividade destes últimos. É importante considerar que a fiebre aftosa non será efectiva para reducir os efectos secundarios dos tratamentos contra o cancro en todos os pacientes e tampouco traballarán para mellorar a eficacia de todas as terapias, pero teñen un gran potencial para facelo polo menos nunha parte e posiblemente. para unha gran parte dos pacientes e medicamentos. Os pacientes fráxiles ou desnutridos ou os pacientes con risco de desnutrición non deben ser inscritos en estudos clínicos de xaxún ou fiebre aftosa, e o estado nutricional e a anorexia dos pacientes deben ser coidadosamente monitorizados ao longo dos ensaios clínicos.
Referencias:
Ámbito de práctica profesional *
A información aquí contenida en "Fasting e cancro: mecanismos moleculares e aplicación clínica" non pretende substituír unha relación individual cun profesional da saúde cualificado ou un médico licenciado e non é un consello médico. Animámoslle a que tome decisións sobre a saúde baseándose na súa investigación e colaboración cun profesional sanitario cualificado.
Información do blog e debates de alcance
O noso ámbito de información limítase a quiropráctica, músculo-esqueléticos, medicamentos físicos, benestar, contribuíndo etiolóxico trastornos viscerosomáticos dentro de presentacións clínicas, dinámica clínica do reflexo somatovisceral asociado, complexos de subluxación, problemas de saúde sensibles e/ou artigos, temas e discusións de medicina funcional.
Proporcionamos e presentamos colaboración clínica con especialistas de diversas disciplinas. Cada especialista réxese polo seu ámbito profesional e a súa xurisdición de licenza. Usamos protocolos funcionais de saúde e benestar para tratar e apoiar a atención das lesións ou trastornos do sistema músculo-esquelético.
Os nosos vídeos, publicacións, temas, temas e coñecementos abarcan asuntos clínicos, cuestións e temas relacionados co noso ámbito de práctica clínica e apoian directa ou indirectamente o noso ámbito de práctica.*
A nosa oficina intentou razoablemente proporcionar citas de apoio e identificou o estudo ou estudos de investigación relevantes que apoian as nosas publicacións. Proporcionamos copias dos estudos de investigación de apoio dispoñibles para os consellos reguladores e o público logo de solicitude.
Entendemos que cubrimos asuntos que requiren unha explicación adicional de como pode axudar nun determinado plan de atención ou protocolo de tratamento; polo tanto, para debater máis sobre o tema anterior, non dubide en preguntar Dr. Alex Jiménez, DC, ou póñase en contacto connosco 915-850-0900.
Estamos aquí para axudarche a ti e á túa familia.
Bendicións
Dr. Alex Jiménez ANUNCIO, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
e-mail: coach@elpasofunctionalmedicine.com
Licenciado como Doutor en Quiropráctica (DC) en Texas & Novo México*
Número de licenza de Texas DC TX5807, New Mexico DC Número de licenza NM-DC2182
Licenciada como enfermeira rexistrada (RN*) in Florida
Licenza Florida Licenza RN # RN9617241 (Nº de control 3558029)
Estado compacto: Licenza multiestatal: Autorizado para Practicar en Estados 40*
Dr. Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
A miña tarxeta de visita dixital